Foto Pixsell
CHMP će svoju ocjenu zaključiti u najkraćem mogućem roku, kada se potvrdi da je cjepivo odgovarajuće u pogledu kakvoće, sigurnosti i djelotvornosti, odnosno kada se utvrdi da su koristi primjene cjepiva veće od rizika.
povezane vijesti
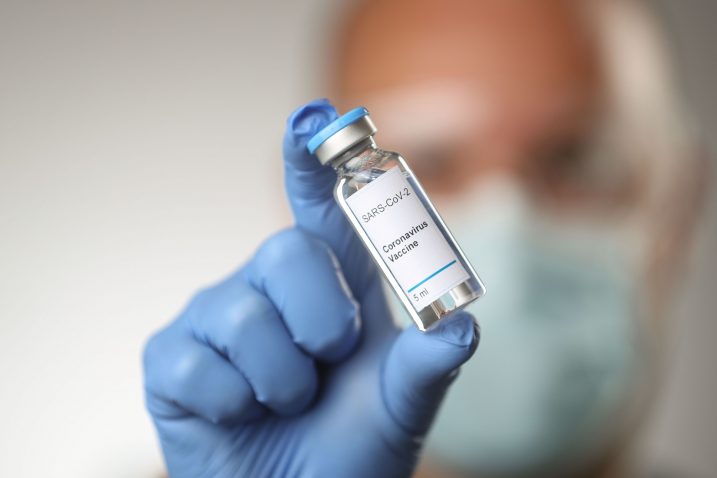
ZAGREB – Hrvatska agencija za lijekove i medicinske proizvode (HALMED) objavila je u utorak da će Povjerenstvo za humane lijekove (CHMP) Europske agencije za lijekove (EMA) na izvanrednoj sjednici 21. prosinca odlučivati o zahtjevu za odobrenje cjepiva protiv covida-19 proizvođača BioNTech i Pfizer.
Povjerenstvo će tada zaključiti svoju znanstveno-stručnu ocjenu tog cjepiva pod uvjetom da na temelju dostavljenih podataka bude moguće provesti temeljitu ocjenu te potvrditi djelotvornost, sigurnost i kakvoću cjepiva.
Sjednica je zakazana nakon što je Povjerenstvo primilo dodatne podatke o cjepivu koje je u postupku ocjene zatražilo od proizvođača.
CHMP će svoju ocjenu zaključiti u najkraćem mogućem roku, kada se potvrdi da je cjepivo odgovarajuće u pogledu kakvoće, sigurnosti i djelotvornosti, odnosno kada se utvrdi da su koristi primjene cjepiva veće od rizika.
Nakon što CHMP preporuči davanje odobravanja za cjepivo, Europska komisija će u sljedećih nekoliko dana ubrzati postupak donošenja odluke s ciljem davanja odobrenja za stavljanje u promet koje će vrijediti u svim državama članicama Europske unije i zemljama Europskog gospodarskog prostora, pa tako i u Republici Hrvatskoj, ističu u HALMED-u
Odobrenje će uključivati i uobičajene mjere opreza, kontrolne mehanizme i obveze. To uključuje potpune informacije o propisivanju te dokumente s detaljnim uputama za sigurnu primjenu, detaljni plan upravljanja rizikom i praćenja sigurnosti, kontrolu proizvodnje, uključujući provjeru kakvoće serija cjepiva i uvjete skladištenja, plan istraživanja za pedijatrijsku populaciju i pravno obvezujuće uvjete nakon davanja odobrenja te jasan pravni okvir za ocjenu novih podataka o djelotvornosti i sigurnosti.
Odobrenje za stavljanje u promet jamči da cjepiva protiv covida-19 udovoljavaju istim visokim europskim standardima kao i sva druga cjepiva i lijekovi. Odobrenje će vrijediti na prostoru cijele EU, što će omogućiti svim državama članicama da istodobno započnu s provođenjem cijepljenja, objavio je HALMED.